セシウムイオンを選択して吸着するタンパク質を発見
![]() 印刷されたい方はこちらをご覧ください
印刷されたい方はこちらをご覧ください ![]() 概要資料はこちらをご覧ください
概要資料はこちらをご覧ください


平成27年3月12日
独立行政法人日本原子力研究開発機構
国立大学法人鹿児島大学
セシウムイオンを選択して吸着するタンパク質を発見
−生物における放射性セシウムの動態を知る新たな手がかり−
| 【発表のポイント】 ・塩濃度が高い環境に生息する細菌が作る特殊なタンパク質の一つ“好塩性βラクタマーゼ”が、セシウムイオンを選択して吸着する部位を持つことを発見。 ・そのセシウムイオン吸着部位の立体構造をX線結晶解析によって解明。 |
独立行政法人日本原子力研究開発機構(理事長 松浦祥次郎。以下「原子力機構」という。)原子力科学研究部門量子ビーム応用研究センター分子構造・機能研究グループの新井栄揮研究副主幹は、国立大学法人鹿児島大学(学長 前田芳實。以下「鹿児島大学」という。)農学部と共同で、好塩性細菌1)が作る好塩性タンパク質2)の一種、好塩性βラクタマーゼ3)(以下「HaBLA」という。)が、セシウムイオンを選択して吸着する部位を持つことを発見しました。
好塩性タンパク質は、高い塩濃度環境に生息する好塩性細菌が作るタンパク質です。好塩性タンパク質は、多数のマイナスの電荷をもつので、希少金属や有害金属も含めた様々な金属イオン(陽イオン)を吸着する部位を有する可能性があると考えました。
これまでタンパク質にはセシウムを選択的に吸着する部位は知られていませんでした。そこで今回の研究では、独自に立体構造解析を行った3種類の好塩性タンパク質にセシウムイオンを添加し、X線結晶解析4)さらにX線の異常分散効果5)を利用して、セシウムイオンが吸着する部位を探しました。そしてHaBLAにセシウムイオンを選択して吸着する部位を発見しました。その立体構造情報6)の特徴を利用すれば、類似した部位を持つタンパク質を探すことができます。これにより、セシウムを吸着しやすいタンパク質を多く持つ生物や生体内の組織、即ち、セシウムを蓄積しやすい可能性がある生物や生体内の組織を探し出すことができます。
今回、好塩性タンパク質は、様々な金属イオンを吸着する立体構造情報を知るために有用な分子であることがわかりました。今後は好塩性タンパク質を利用した希少金属の捕集材料開発の可能性も検討する予定です。
本研究成果は、2015年2月26日に「Acta Crystallographica Section D」に掲載されました。
研究開発の背景と目的
タンパク質は生物の生命活動のために、金属イオンの電荷数7)の違いやイオン半径8)のわずかな違いを識別して結合するなど、緻密な仕組みを有します。多くのタンパク質が必須元素9)の金属を結合することは広く知られていますが、タンパク質が必須元素ではないセシウムを選択して吸着しうるのか、また、その吸着部位はどのような構造をしているのか等は明らかにされていませんでした。特に、東京電力株式会社福島第一原子力発電所事故によって放出された放射性セシウムの生物への影響を知るためにも、タンパク質におけるセシウムイオンの吸着のしやすさや吸着部位の構造を解明することは重要と考えられます。
そこで、本研究では好塩性タンパク質に着目しました。好塩性タンパク質は、死海のような塩湖・岩塩・塩蔵食品・発酵食品などの塩濃度が高い環境に生息する好塩性細菌が作るタンパク質です。好塩性タンパク質は、塩濃度が高い環境に適応するために多く酸性アミノ酸10)を含有し、多くのマイナスの電荷を有することから、セシウムイオンを含む様々な金属イオンを吸着する可能性があります。本研究では、好塩性タンパク質の中でも比較的高い酸性アミノ酸含量を有し(表1)、且つ、大腸菌への遺伝子組換え11)によって大量に作ることが可能なHaBLAについて、立体構造の解明とセシウムイオンの吸着部位の検出を試みました。
HaBLAを作るために必要な遺伝子の作製は鹿児島大学が担当し、HaBLAの結晶の作製やX線結晶解析およびHaBLAに結合したセシウムイオンの検出は原子力機構が担当しました。
【表1】好塩性βラクタマーゼと通常のβラクタマーゼに含まれるアミノ酸の比較
| HaBLA (好塩性βラクタマーゼ) |
EaBLA (通常のβラクタマーゼ) |
|
|---|---|---|
| 細菌 | Chromohalobacter sp.560 (好塩性細菌) |
Enterobacter aerogenes (通常の細菌) |
| 酸性アミノ酸の数(個) (アスパラギン酸 + グルタミン酸) |
32 + 25 | 12 + 17 |
| 塩基性アミノ酸の数(個) (アルギニン + リジン) |
18 + 9 | 13 + 18 |
| 酸性アミノ酸含量(個/個) (酸性アミノ酸の数 / 塩基性アミノ酸の数) |
2.11 | 0.94 |
研究の手法と成果
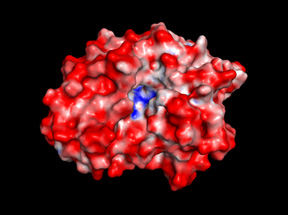
本研究では、まず、高エネルギー加速器研究機構・フォトンファクトリー12) (PF)のX線結晶回折装置NE3Aを用いて、X線結晶解析法によりHaBLAの立体構造を解明しました。その結果、HaBLAの分子表面は、ほとんどが負電荷で占められ、多くの金属イオン吸着部位を有する可能性が明らかになりました(図1)。
続いて、HaBLA結晶に、セシウムイオンを加えてX線の異常分散効果を測定し、HaBLAに吸着したセシウムイオンを検出するとともに、その吸着部位の構造を調べました。X線の異常分散効果によるセシウムイオンの検出は、佐賀県立九州シンクロトロン光研究センター13)のビームラインBL07に設置されたX線結晶回折装置を利用して行いました。その結果、HaBLA分子上にセシウムイオン吸着部位を発見しました。更に、今回発見したセシウムイオン吸着部位は、セシウムイオンに似た性質を有するナトリウムイオン14)がセシウムイオンよりも9倍多く含まれる溶液(濃度0.09 mol/Lのナトリウムイオンと0.01 mol/Lのセシウムイオンが混在する溶液)でも、セシウムイオンを選択して吸着することが明らかになりました(図2)。本研究により、タンパク質にセシウムを選択して吸着する部位が存在することが初めて明らかになりました。また、分子量15)約4万のHaBLA一分子に原子量16)132.9のセシウムが一個吸着することから換算して、1 kgのHaBLAによって約3 gのセシウムを吸着すると見積もられました。
|
|
【図1】HaBLAの分子表面 金属イオンの吸着に寄与する多くの負電荷(赤)が存在することが明らかになった。 |

【図2】左:HaBLAに結合した金属イオン。 右:セシウムイオン吸着部位の拡大図。
青の網掛はセシウムイオンの電子密度。この部位は、トリプトファン(W189)のベンゼン環、および、グルタミン(Q186)とトレオニン(T188)の主鎖の酸素(O)によって構成されることが明らかになった。
今後の予定
本研究で発見したセシウムイオン吸着部位の立体構造情報を利用すれば、類似した部位を持つタンパク質、即ち、セシウムイオンを吸着しやすいタンパク質を探すことができます。このことは、放射性セシウムを吸収しやすい生物を調べるための新たな手掛かりとなります。さらに、好塩性タンパク質には、セシウムイオン以外の金属イオンの吸着部位も存在する可能性があります。リチウムイオンなどの希少金属イオンを選択して吸着する部位をタンパク質分子上に探し出せば、希少金属を捕集する新たな材料を創製できる可能性もあります。今後、好塩性タンパク質を利用して様々な希少金属・有害金属の吸着部位を探し出し、吸着方法の違いを調査します。
用語説明
1) 好塩性細菌
塩環境に適応するとともに塩を生育に要求する細菌。生育する塩濃度によって大まかに、高度好塩菌(塩濃度20% 以上)、中度好塩菌(塩濃度5〜20%)、低度好塩菌(塩濃度2〜5%)に分類できる。HaBLAを作る好塩性細菌Chromohalobacter sp.560は、中度好塩菌である。
2) 好塩性タンパク質
好塩性細菌が作り出すタンパク質であり、その安定性や酵素活性などの機能のために塩を必要とする。
3) βラクタマーゼ
抗生物質の一種であるβ‐ラクタム系抗生物質を分解する酵素。
4) X線結晶解析
結晶にX線を当てると、結晶中に規則正しく並んだ原子のそばをX線が通過するときに曲がり込み(回折)が生じる。回折したX線は、結晶中の原子の配置に対応した様々な強度の点をとして観測することができる。この点の分布と強度から、元の結晶中の原子の分布を求める解析をX線結晶解析と呼ぶ。
5) X線の異常分散効果
原子の種類によって、特定の波長域のX線の回折や吸収が不連続的に大きく変化する現象。結晶を用いてX線の異常分散効果を測定すると、結晶中における特定の原子の種類や位置を正確に調べることができる。
6) タンパク質の立体構造情報
タンパク質分子を構成する原子の三次元的な位置の情報。
7) 電荷数
イオンや素粒子が有する電荷の数。セシウムイオンやナトリウムイオンは正電荷を一つ持つため、+1と表記する。
8) イオン半径
イオンを球と仮定した場合の半径。
9) 必須元素
生物が生命維持するために不可欠な元素。金属元素では、主にナトリウム、マグネシウム、カリウム、カルシウム、鉄など。
10) 酸性アミノ酸
側鎖と呼ばれる部分が酸性の性質を持ち、負電荷を有するアミノ酸。グルタミン酸,アスパラギン酸など。
11) 遺伝子組換え
遺伝子を人工的に操作すること。
12) フォトンファクトリー
茨城県つくば市の高エネルギー加速器研究機構に設置されている大型放射光施設。
13) 佐賀県立九州シンクロトロン光研究センター
佐賀県が設置した産学官共用型の放射光施設(佐賀県鳥栖市)。
14) ナトリウムイオン
ナトリウムはセシウムと同じ第一族元素である。周期表上の同じ族の元素は、似た性質を有する。例えばナトリウムイオンの電荷数はセシウムイオンの電荷数と同じ+1であり、電気的な性質が似ている。また、ナトリウムイオンのイオン半径は約1.16 Å(1 Åは10-10m)、セシウムイオンのイオン半径は約1.81 Åであり、イオン半径の違いはわずか0.65 Å程度である。
15) 分子量
分子中に含まれる原子量の総和。
16) 原子量
炭素の質量を12とし、そこから相対的に他の原子の質量を表した値。タンパク質を構成する原子の原子量は、水素が1.0、炭素が12.0、窒素が14.0、酸素が16.0、硫黄が32.1となる。また、本研究で用いたセシウムの原子量は132.9である。
本件に関する問合せ先
独立行政法人日本原子力研究開発機構
(研究内容について)
原子力科学研究部門 量子ビーム応用研究センター
量子ビーム機能性分子解析技術研究ユニット 分子構造・機能研究グループ 研究副主幹 新井 栄揮
TEL:029-282-6727, FAX:029-282-5822
(報道担当)
広報部報道課長 中野 裕範
TEL:03-3592-2346, FAX:03-5157-1950
鹿児島大学に関する問合せ先
鹿児島大学 広報センター TEL:099-285-7035 FAX:099-285-3854
佐賀県立九州シンクロトロン光研究センターに関する問合せ先
公益財団法人佐賀県地域産業支援センター 九州シンクロトロン光研究センター 利用企画課
TEL: 0942-83-5017, FAX: 0942-83-5196